


Calor latente é a grandeza física que determina a quantidade de calor que uma unidade de massa de determinada substância deve receber para mudar de estado físico. No Sistema Internacional de Unidades (SI), a unidade é J/kg (Joule por quilograma). Outra unidade usual é caloria por grama (cal/g).
Para calcular o calor latente de uma subtância, basta dividir a quantidade de calor Q que a substância precisa ganhar ou perder para mudar de fase pela massa m da mesma.

Temos que L é o calor latente em cal/g.
É possível calcular o calor específico de uma substância ( ) a partir da capacidade térmica de um corpo composto por ela (
) a partir da capacidade térmica de um corpo composto por ela (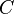 ) e da massa desse corpo (
) e da massa desse corpo ( ).
).
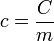
Também é possível determinar o calor específico de uma substância a partir da quantidade de calor cedida a um corpo dessa substância (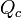 ), da variação térmica que ele sofre (
), da variação térmica que ele sofre ( ), e da massa desse corpo.
), e da massa desse corpo.
