Um gás é o conteúdo da fase gasosa, no qual a matéria tem forma e volume variáveis. Nos gases, as moléculas se movem livremente e com grande velocidade. A força de coesão é mínima e a de repulsão é enorme.
Por razões didáticas, a Física classifica os gases em duas categorias:
- os gases perfeitos ou ideais
- os gases reais
Na verdade, nenhum gás é perfeito. Só pode ser tratado como tal, um gás em muito baixa pressão e temperatura.
Lei de Gay-Lussac
Dentro do âmbito da Química e da Física a Lei de Gay-Lussac é uma lei dos gases perfeitos: sob volume constante, a pressão de uma quantidade constante de gás aumenta proporcionalmente com a temperatura:
ou
onde:
- P é a pressão do gas.
- T é a temperatura do gas (em kelvins).
- k é uma constante.
Para comparar a mesma substância en dois tipos de condições:

- Lei de Charles
A Lei de Charles é uma lei dos gases perfeitos : à pressão constante, o volume de uma quantidade constante de gás aumenta proporcionalmente com a temperatura.
Esta lei diz respeito às transformações isocóricas ou isométricas, isto é, aquelas que se processam a volume constante, cujo enunciado é o seguinte:
O volume constante, a pressão de uma determinada massa de gás é diretamente proporcional à sua temperatura absoluta, ou seja: = constante
Desta maneira, aumentando a temperatura de um gás a volume constante, aumenta a pressão que ele exerce, e diminuindo a temperatura, a pressão também diminui. Teoricamente, ao cessar a agitação térmica das moléculas a pressão é nula, e atinge-se o zero absoluto.
A representação gráfica da transformação isométrica é uma reta.
Lei de Boyle-Mariotte
A Lei de Boyle-Mariotte (enunciada por Robert Boyle e Edme Mariotte) diz que:
"Sob temperatura constante (condições isotermas), o produto da pressão e do volume de uma massa gasosa é constante, sendo, portanto, inversamente proporcionais. Qualquer aumento de pressão produz uma diminuição de volume e qualquer aumento de volume produz uma diminuição de pressão."
Em um gráfico pressão x volume, sob uma temperatura constante, o produto entre pressão e volume deveria ser constante, se o gás fosse perfeito. Existe uma temperatura onde o gás real aparentemente obedece à lei de Boyle-Mariotte. Esta temperatura é chamada de temperatura de Mariotte.
Transformações isotérmicas nos gases perfeitos
Em uma transformação isotérmica, envolvendo um gás perfeito, o produto entre pressão e volume é constante. É possível calcular a pressão e o volume desse gás através da fórmula:

Nessa fórmula,  e
e  são as pressões inicial e final, respecivamente. Da mesma forma,
são as pressões inicial e final, respecivamente. Da mesma forma,  e
e  são os volumes inicial e final.
são os volumes inicial e final.
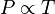
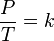





 ) a partir da capacidade térmica de um corpo composto por ela (
) a partir da capacidade térmica de um corpo composto por ela (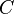 ) e da massa desse corpo (
) e da massa desse corpo ( ).
).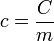
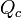 ), da variação térmica que ele sofre (
), da variação térmica que ele sofre ( ), e da massa desse corpo.
), e da massa desse corpo.



